マレーシア化粧品申請

MALAYSIA
マレーシア化粧品について
マレーシアにおける化粧品監督官庁
国立医薬品規制機関(NPRA)は、マレーシアの規制当局であり、医薬品、健康補助食品、伝統的製品、化粧品の品質、安全性、有効性を確保します。
製品通知申請の基本的な流れ
製品の成分および表示がマレーシアの規制およびガイドラインに準拠しているかどうかを確認する。
必要な情報:
化粧品名
製品種別
製品形態 (例: シリーズか単独製品か)
成分表 %
・INCI名とCAS番号
・CI番号(着色料)
生産企業情報(住所、電話番号など)
輸入企業情報(住所、電話番号など)
補足情報(ある場合)
必要な資料
GMP証明書
パッケージ/ラベルデータ
授権書 (LOA) (公証認証)
当局による書類審査期間:約3−4ヶ月
PIF(Product Information File)= 製品情報ファイル
フィリピンは、製品を市場流通させている個人または企業が、PIFを保管し、規制当局からの要求があり次第、提示ができる様にすることを義務づけている。
マレーシアPIFについて
PIF保管者:
化粧品通知ホルダー(CNH:Cosmetic Notification Holder)を担う企業。
PIF保管場所:
CNHの管轄で、データまたは書面で保管がされる。
PIFの提出:
製品の市場監査の際やCNHへのランダムなPIF保持調査 等
消費者からの有害事象報告があった場合、内容に応じてPIFの提出要求がある
PIF作成・保管方法:
PIFは、製品流通後少なくとも3年間*、書面または電子データで保存
言語:マレー語または英語
製品情報に変更・更新がある場合、PIFに追加をする必要がある
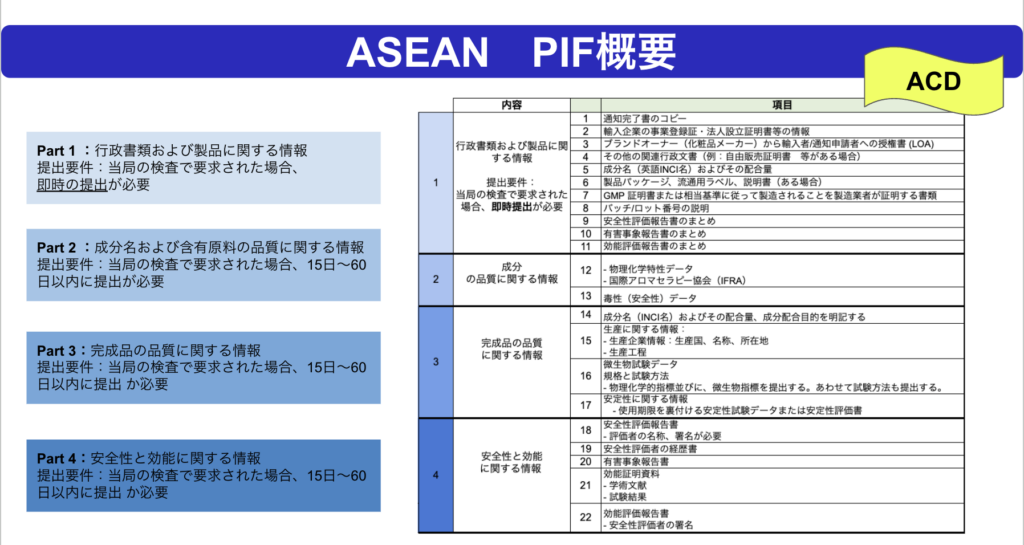
PIFの要求資料
お問い合わせ
お気軽にお問い合わせください。3営業日以内にご返答させて頂きます。
<本件に関するお問い合わせ>
株式会社WWIPコンサルティングジャパン
TEL : 03-6206-1723
Email: official@wwip.co.jp




