台湾PIF制度とWWIPの取り組み
皆様ご存知のとおり、2024年7月1日から台湾PIF制度が開始されました。まずは、2024年7月に特別用途化粧品が対象となり、その後は2025年、2026年と続きます。台湾当局である台湾衛生福利部食品薬物管理署(以下「台湾FDA」)にとっても非常に大きな変革であり、今後の市場監査の強化等が予想されます。
新しく始まる台湾PIF制度とは?PIF開始の背景と目的
2024年7月以降、台湾では、化粧品を供給・販売・寄贈・公開陳列或いは消費者に試供品として提供する前に、製品情報ファイル(Product Information File, PIF)を作成、保管することが求められています。製品に健康上の危害及び安全性を憂慮される事態が生じた場合、または台湾FDAによる監査の際に、PIFを提出が必要です。
PIF制度は、今までもEUやアセアンで既に行われているが、台湾PIFはEUからの影響を受けつつも台湾独自の規制を作りあげています。
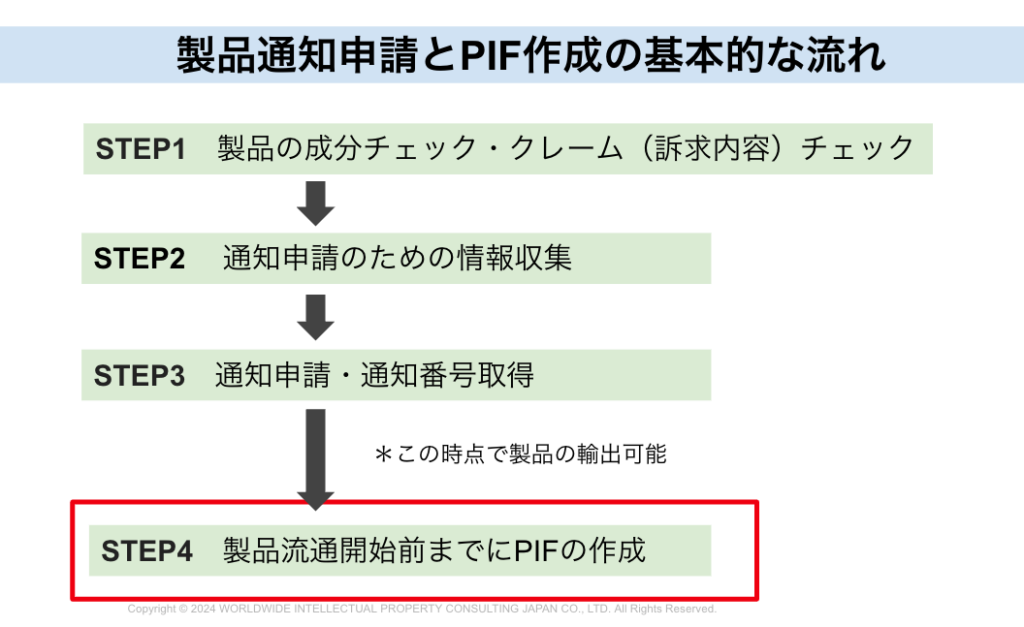
PIF制度の段階的導入
〜 2021年7月から施行された新たな通知システム 〜
台湾のPIF制度は、2018年に発表された台湾の包括的な化粧品規制「化粧品衛生安全管理法」で規定されました。
本規程は化粧品に対する規制を強化するものであり主に3点のポイントに集約されます。
● 2021年7月より、台湾に既に流通する製品、今後流通する全ての 一般化粧品を対象にした、新たな通知システムの開始がされた。
● 2024年7月には、今まで登録・審査が必要とされていた 特別用途化粧品にも通知システムが導入される。
● 全ての化粧品に対して、市場に流通する前にPIFの備え置きを義務づける制度が導入される。
– 目的 –
輸出のための事前承認手続きが簡素化される代わり、化粧品業界の自主管理を強化し、各社が責任をもって製品の品質を向上させ、消費者の安全を守るため PIF制度が開始されることが決まりました。
台湾独自に制定する安全性評価者への要求とは?
安全性評価者とは、台湾が制定する資格を持ち合わせている者のみが担当することができ、製品の安全性を結論付ける役割を持ちます。PIF(製品情報ファイル)の全ての内容を精査、確認し、製品の安全性を評価します。
↑化粧品製品情報ファイル管理辯法に安全性評価者の資格が記述されています。
台湾化粧品安全性評価者になるための条件
WWIPの有資格安全性評価者のご紹介
弊社では、台湾国内大学に通学し安全性評価者の資格取得をしたスタッフが在籍しております。
台湾PIFの作成から安全性評価までワンストップでサポート可能です。

台湾特独の認証制度の条件を満たす者である必要がある。
EU、アセアン、中国などの安全評価資格保持者であっても、
加えて台湾の安全性評価資格の条件を満たす必要があるので、注意が必要。
台湾PIF資料1〜16とは?
台湾FDAの発行する化粧品情報ファイル管理規制、及び化粧品製品情報ファイル作成入門マニュアルとガイドラインに、要求資料1-16の内容が記されています。PIF作成の進め方としては、1-15の書類を収集し全ての書類を安全性評価者が精査することで16の項目が完了します。

弊社が推奨する着手の順番としては、まずは項目9・10に着手し、成分の安全性資料を収集することです。
9・10の内容が集まれば安全性評価者はMoS算出を含め、安全性評価が可能かの確認をすることが可能です。
併せて、安定性試験結果、微生物試験結果、保存効力試験結果、効能エビデンスを持っているか、それが台湾の要求を満たしているかを事前に確認する必要があります。項目1-8、11-15の収集について条件を満たした試験結果や資料等があるという状況を確認ができていれば、内容のチェックは、項目9・10と同時進行または後手にしても、大きな問題はありません。
*安全性評価者により判断が異なる場合がありますので、事前にご確認ください。
WWIPでのPIF作成期間の目安:
お客様の資料収集期間を含み、安全性評価実施、署名までスムーズなケースで4〜6ヶ月程でご案内しております。
しかし、資料収集に工数がかかってしまうケースが多く発生しておりますため、製品数が多い場合は余裕を持ってご依頼ください。
お急ぎの場合は、より期間を短縮することも可能ですのでご相談ください。
日本企業に求められる対応
WWIPでは、現時点(2024年7月)で98製品のPIF作成を行い、安全評価を実施してまいりました。
その中でも、日本企業にとって最もハードルが高いと言える要求が、台湾TFDAが安全性評価者に求める資格であり、また、全ての配合成分に対する安全評価が要求されているという点です。
PIF制度導入は、企業が責任をもって製品の安全性等の管理(=PIFの作成、保管と更新)を行うことが前提となっており、当局の事後監査が強化されることも視野に、PIF要求に真摯に対応をする必要があります。

WWIPの台湾PIFセミナー 講師実績
- 2023年11月30日 WWIP主催
台湾PIF制度カウントダウン:2024年7月までに迫られる対応と最新情報解説セミナー - 2024年1月17日 Cosme Week 2024 東京様主催
ASEAN・台湾における最新の化粧品申請制度と申請を円滑に進める重要ポイント! - 2024年5月9日 WWIP主催
開始直前!今からでも間に合う台湾PIF制度理解促進セミナー【入門】 - 2024年5月24日 サイエンス&テクノロジー(株)様主催
ASEAN・台湾の最新化粧品申請制度解説 - 2024年6月11日 WWIP主催
開始直前!台湾PIF制度理解促進セミナー【総復習編】 - (予定)2024年8月7日 (株)情報機構様主催
台湾化粧品のPIF制度 入門セミナー - (予定)2024年10月7日 様主催
〜中国化粧品安全評価報告<完全版>・企業査察に関する最新情報と遂に開始された台湾PIF制度概要と現状報告〜
WWIP主催自社セミナーは、動画データをご視聴いただくことが可能です。
株式会社ワールドワイド・アイピー・コンサルティングジャパンでは、台湾の成分や効能訴求規制調査、通知申請、そして台湾PIF作成サポートを提供しております。WWIPコンサルタントへお気軽にお問い合わせください。
<本件に関するお問い合わせ>
株式会社WWIPコンサルティングジャパン
TEL : 03-6206-1723
Email: official@wwip.co.jp





